![]()
Caract?ristiques
g?n?rales des deux ?tapes de la dépollution azot?e : La nitrification
et la d?nitricication.
Article de la société PRODIBIO
LE PRINCIPE DE BASE DE l'EPURATION BIOLOGIQUE :
La
possibilit? de maintenir un aquarium en bonne sant? est fonction de l'efficacit?
de l??puration des eaux pollu?es de l'aquarium. Ceci est rendu possible
par le travail biologique accompli par des ?quipes de bact?ries b?n?fiques
qui travaillent en synergie dans un environnement qui leur convient.
L'?puration biologique tend ? ?liminer les polluants de l'aquarium. Elle
les transforme et les m?tabolise en mati?re vivante: Biomasse bact?rienne,
micro-plancton, invert?br?s, plantes, augmentation du poids des poissons.
Ces polluants sont le r?sultat :
- - des sous-produits des d?jections des organismes vivants : urine, excr?ments...
- - des restes de nourriture.
- - de la d?composition de cadavres et de plantes ...
LE CYCLE DE L'AZOTE EN AQUARIUM
Dans un aquarium, l'ensemble des r?actions biologiques de croissance et de maintenance requiert
la pr?sence de l'?l?ment azote : N. C'est un ?l?ment fondamental de la mati?re vivante.
L'introduction de nourriture augmente la quantit? totale d'azote dans ce milieu ferm? qu'est l'aquarium.
 |
|
L'azote
min?ral est assimil? par les bact?ries et par les v?g?taux, (phytoplancton
et plantes sup?rieures) pour la fabrication des mati?res v?g?tales. Ces
prot?ines v?g?tales entrent ensuite directement (herbivores) ou indirectement
(carnivores) dans l'alimentation des animaux.
Les compos?s azot?s organiques vont donc se retrouver dans les urines, les
excr?ments et les cadavres. Ils seront ? leur tour d?grad?s par ces bact?ries
bien d?finies, en compos?s ammoniacaux, nitrites et enfin en nitrates .
Ainsi se trouve r?sum?, tr?s sch?matiquement, LE CYCLE DE L'AZOTE
qui se renouvelle ind?finiment.
D?composition
des nitrates
Certaines souches bact?riennes vont ?tre capable de puiser l'oxyg?ne n?cessaire
? leur multiplication dans l'oxyg?ne dissout dans l'eau. D?autres sous
certaines conditions de stress ou d'anoxie sont ? m?me de puiser cet oxyg?ne
dans les nitrates, pour les transformer en azote gaz qui est sans danger en
aquarium et s'?vacue dans l'atmosph?re.
Il est par cons?quent facile de comprendre que le contr?le de ces produits,
dont certains sont extr?mement toxiques, soit tr?s important dans la conduite
d'un aquarium.
SEUILS DE MORTALITE EN AQUARIOPHILIE
|
Ammoniac
|
(NH3)
|
0.1 mg/l
|
ne pas d?passer 0.01 mg/l
|
|
|
Ammonium
|
(NH4+)
|
peu toxique, sa toxicit? d?pend du pH
|
voir tableau
|
|
|
Nitrites
|
(NO2-)
|
0.5 mg/l
|
ne pas d?passer 0.1 mg/l
|
|
|
Nitrates
|
(NO3-)
|
50 mg/l
|
Invert?br?s marins
|
ne pas d?passer 5 mg/l
|
|
500 mg/l
|
Poissons
|
variable selon les espèces
|
||
L'AMMONISATION
La premi?re ?tape de la d?gradation des d?chets azot?s organiques est l'ammonisationgr?ce ? des micro-organismes des genres Bacillus, Azotobacter, Micrococcus... Elle va produire des compos?s ammoniacaux NH3 et NH4+ dont la toxicit? est variable selon le pH. En aquariophilie les tests utilis?s permettent
une mesure de la toalit? (NH3 + NH4+) L'ion NH4+ n'est pas toxique. Malheureusement, il a tendance ? se transformer, en m?me temps que le pH s'?l?ve, en ammoniac tr?s toxique. Un abaissement du pH provoque
la r?action inverse, et ceci peut se r?p?ter ind?finiment.Tableau donnant le pourcentage d'ammoniac en fonction du pH ? 25?
| pH | 6,5 | 7 | 7,5 | 8 | 8,5 | 9 | 9,5 |
| NH3(%) | 0,2 | 0,6 | 1,7 | 5,3 | 15 | 36 | 64 |
Exemple
R?sultat du test ammonium: 1,5mg/l pH 7 donc NH3 = 1,5 x 0,6%
= 0,009 peu toxique.
Il n'en est pas de m?me si le pH remonte ? 8 par exemple Pour pH 8 NH3
= 1,5 x 5,3 % = 0,08 Tr?s toxique
Faire tr?s attention aux remont?es de pH dans les sacs d'eau de mer apr?s
un long s?jour lors d'importations.
Quelques grammes de z?olites - Clinoptilolite - dans les sacs peuvent rendre
de tr?s grands services.
LA NITRIFICATION
La nitrification est la transformation des compos?s azot?s en ?lements dont l'azote est dans l'?tat le plus oxyd? :
LES NITRATES. Elle est assur?e par des bact?ries autotrophes (capables de se d?velopper ? partir des seuls
?l?ments min?raux), et des bact?ries nitrifiantes h?t?rotrophes (capables de se d?velopper ? partir de substances issues de tissus vivants). La part la plus importante de la nitrification dans un ?cosyst?me est g?n?ralement attribu? aux microorganismes autotrophes a?robies stricts appartenant ? la famille des Nitrobacteriaceae: Nitrosomonas (ammonium - nitrites) et Nitrobacter (nitrites - nitrates).
Les bact?ries nitrifiantes utilisent l'azote ammoniacal ou les nitrites comme source d'azote et comme source d'?nergie (donneurs d'?lectrons). Les source de carbone sont le gaz carbonique et les carbonates.
Les organismes nitrifiants h?t?rotrophes utilisent une source de carbone organique comme source d'?nergie
et oxydent des compos?s azot?s organiques ou inorganiques.La r?action se d?compose en deux ?tapes :
- la nitritation ou nitrosation (oxydation de l'azote ammoniacal en nitrites).
- la nitratation (oxydation des nitrites en nitrates).
Plusieurs facteurs principaux affectent le processus de nitrification : La physico-chimie de l'eau, la concentration en oxyg?ne, les oligo-?l?ments et la communaut? biologique.
Physico-chimie de l'eau :En pr?sence de compos?s ammoniacaux, les bact?ries de la cha?ne de nitrification vont se multiplier. Cependant cette multiplication d?pend souvent des conditions du milieu.
En effet la croissance des Nitrobacter est inhib?e lorsque le taux d'ammoniac est trop ?lev? (sup?rieur ? 0,1mg/l de NH3). Faute d'une quantit? suffisante de Nitrobacter un taux ?lev? de nitrites sera mesur? alors que le taux d'ammonium ne permet pas aux Nitrobacter de cro?tre, rallongeant ainsi la dur?e de maturation du filtre biologique. Il ne faut pas oublier que les bact?ries se livrent ? une terrible comp?tition, d'autant plus nuisible ? l'?tablissement du filtre biologique que les conditions sont mauvaises : manque d'oxyg?ne, de certains oligo-?l?ments, abaissement anormal du pH, exc?s de pollution, etc.?
Ceci se traduit dans l'aquarium par des eaux troubles, r?sultats des luttes bact?riennes, avec prolif?rations anarchiques de bact?ries de pleine eau.Le pH ;
Equations de principe :
2NH4+ + 3 O2 >> 2NO2- + 4H+ + 2H2O 2NO2- + O2 >> 2NO3-
2NH4+ + 3 O2 + 2NO2- + O2 >> 2NO2- + 2NO3- + 4H+ + 2H2O soit 2NH4+ + 3 O2 + O2 >> 2NO3- + 2H2O + 4H+
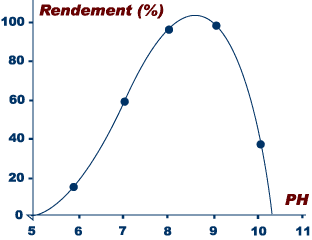
Rendement de la nitrification en fonction du pH :
La nitrification lib?re des ions H+ et abaisse
donc le pH qui doit ?tre suivi surtout au d?marrage des aquariums.
La pr?sence de carbonates procure un effet
tampon contre les variation de pH.
Le pH optimal pour la nitrification se situe autours de 8,0. Les valeurs hors du champ 6,8 -8,6 peuvent affecter l'efficacit? de la nitrification.
On voit bien que la nitrification :
1. - Consomme de l'oxyg?ne
2. - acidifie le milieu en lib?rant des ions H+La temp?rature
La température a un effet important sur les vitesses de croissance.
Entre 23? et 30? le taux de croissance maximal est multipli? par 4 pour Nitrosomonas. La temp?rature optimale se situe entre 30? et 36? (Knowles et al., 1965). Ce taux augmente d'environ 6% par degr? centigrade pour Nitrobacter. La temp?rature optimale étant de 28?. Le taux de d?gradation des mati?res peut diminuer de moiti? pour une diminution de 10?
La concentration en oxyg?neL'oxyg?ne est un facteur de la r?action d'oxydation. En cas de mauvaise oxyg?nation, il peut donc appara?tre comme un facteur limitant.
Or les constantes de demi-saturation par rapport ? l'oxyg?ne dissout vont pour Nitrosomonas, de 0,25 ?1,3mg/l, et de 0,5 ?1mg/l pour Nitrobacter selon la temp?rature (Capdeville, 1991 ).
Ceci indiquerait qu'il n'est pas n?cessaire de maintenir des concentrations ?lev?es en oxyg?ne dissout dans les syst?mes nitrifiants : 4mg/l seraient suffisant.
Cependant, comme c'est le cas en aquarium, la concentration en oxyg?ne devient primordiale lorsqu'il y a comp?tition entre une flore h?t?rotrophe, et une flore autotrophe surtout en pr?sence de carbone. En effet les bact?ries h?t?rotrophes inhibent les micro-organismes nitrifiants avec lesquelles elles sont en comp?tition pour l'oxyg?ne et l'azote ammoniacal car elles poss?dent un taux de croissance maximal cinq fois sup?rieur
? celui des autotrophes. Ceci explique la n?cessit? d'une bonne oxyg?nation et d'une communaut?
de souches bact?riennes soigneusement d?termin?e.
LA PRESENCE D'ELEMENTS DE TRACE
En
aquarium l'ammoniac et les nitrites ne sont pour les bact?ries, qu?une
source d'azote. D'autres ?l?ments nutritifs, comme les ?l?ments de trace,
sont n?cessaires pour la multiplication des bact?ries ?puratoires et pour
?liminer ammoniac, nitrites, nitrates et phosphates. La capacit? d'accomplir
la d?nitrification compl?te est subordonn?e ? la pr?sence d'?l?ments
de trace essentiels. BLASZCZYK (1993) a montr? que l'addition d'?l?ments
de trace essentiels multipliait la d?nitrification par 10.
Les ?l?ments
de trace sont n?cessaires ? la vie de tous les organismes. Ceci s'?tend
du Souffre pour les prot?ines, au Fer pour les plantes et le
sang des poissons, du Cobalt pour les vitamines B au Bore pour
les nombreux produits du m?tabolisme - anabolisme et catabolisme - au cours
des ph?nom?nes d'?dification des tissus et de d?gradations organiques.
Ils sont
?galement n?cessaires pour le travail des bact?ries.
En aquarium,
les oligo-?l?ments essentiels, indispensables ? toute activit? biologique,
sont consomm?s par la d?gradation des d?chets, les algues, les plantes,
les invert?br?s... et neutralis?s ou ?limin?s par l'?cumeur, le charbon
actif.
L'eau osmos?e
utilis?e de plus en plus souvent ? cause des nitrates n'en contient pas
du tout. On observe alors des carences d'?l?ments de trace qui peuvent stopper
toutes les fonctions bact?riennes. Cela provoque un ralentissement g?n?ral
de l'?puration : Eau terne, prolif?ration d'algues, poissons amorphes, plantes
ch?tives.. L?ajout d?une solution contenant les ?l?ments de trace essentiels,
agit comme un catalyseur biologique, favorise la multiplication des bact?ries
?puratoires et la production d'enzymes pour dig?rer les d?chets de l'aquarium.
LA COMMUNAUTE BIOLOGIQUE
Lors de l'installation d'un aquarium on peut consid?rer que le milieu nouvellement cr?e est vierge de bact?ries. Ces bact?ries qui sont pr?sentes partout vont coloniser ce milieu en fonction des apports dans l'aquarium : Substrat, plantes, nourriture, peuplement... et au hasard de la concurrence alimentaire pour les diff?rentes souches. C'est le hasard seul qui va organiser cette multiplication bact?rienne dans l?aquarium. Toutes les bact?ries vont vouloir s'y d?velopper et ce ne sera pas toujours les bact?ries b?n?fiques qui vont se d?velopper le plus rapidement. Cela risque de provoquer la lutte de souches bact?riennes de pleine eau, ce qui provoque une eau poussi?reuse, et un retard dans l'?quilibre biologique de l'?puration.
LA NITRIFICATION HETEROTROPHE
L'activit? nitrifiante des bact?ries h?t?rotrophes - qui utilisent comme principale nourriture du carbone organique, issu de mati?res vivantes - est effective mais ? une vitesse beaucoup plus faible que celle observ?e pour des autotrophes. Ils sont appel?s les Nitrifiants pauvres. ls sont n?anmoins n?cessaire car ils d?gradent des compos?s azot?s allant de l'azote ammoniacal aux compos?s de la cha?ne aliphatique (graisses) ou aromatique ainsi que des sous-produits de la nitrification : hydroxylamine, oxyme, acide hydroxamique... L'observation de la production des nitrites et des nitrates lors du travail de ces bact?ries montre que tr?s peu d'oxydes d'azote s'accumulent. Il a ?t? d?montr? que tous les nitrifiants h?t?rotrophes, et parmi ceux-ci Paracoccus denitrificans, Pseudomonas stuzerii..., sont des d?nitrifiants a?robies, ce qui expliquerait la non-accumulation des nitrites et des nitrates lorsque la communaut? bact?rienne est bien d?finie et qu'elle travaille efficacement (Papen et al., 1989, Van Niel et al., 1992a). Il est ainsi possible de transformer la pollution azot?e ammoniacale en azote mol?culaire au sein d'un m?me micro-organisme.
LA DENITRIFICATION, L'EPURATION BIOLOGIQUE
La d?nitrification est d?finie comme ?tant ?tant la transformation des nitrates en azote gazeux avec pour interm?diaire le nitrite, l'oxyde nitrique, l'oxyde nitreux, chacun ?tant r?duit par une enzyme r?ductase s?cr?t?e par les bact?ries concern?es.
| NAR | NIR | NOR | N2 OR | |||||
| NO3- | ------ | NO2- | ------ | NO | ------ | N2O | ------ | N2 |
Etapes de la d?nitrification :
Interm?diaires et enzymes.
NAR = nitrate r?ductase NIR = nitrite r?ductase NOR = oxyde nitrique r?ductase
N2 OR = oxyde nitreux r?ductase
Chaque interm?diaire est r?duit par une enzyme secr?t?e par les bact?ries concern?es.
L??quation montre que la d?nitrification g?n?re des ions hydroxydes b?n?fiques en eau de mer.
13 N03- + 6(C2H5OH) A 6,5 N2+15H2O+12CO2+6(OH)
La d?nitrification est une alternative ? la respiration classique de l'oxyg?ne dans les zones peu oxyg?n?es
de l'aquarium. L'oxyg?ne peut ?tre aussi - moins facilement - puis? dans les nitrates ou l'un des interm?diaires. Dans des conditions de stress ana?robie - ce qui est la cas dans la mise en ampoules sous azote - on provoque, chez certaines bact?ries a?robies/ana?robies facultatives, la production pendant un certain temps des enzymes r?ductases de la d?nitrification. La r?duction des nitrates est coupl?e ? l'oxydation :- soit de compos?s min?raux comme le soufre, avec Thiobacillus denitrificans
- soit de compos?s carbon?s organiques, Bacillus azotoformans, Bacillus aminovorans...
En
aquarium, en eau douce comme en eau de mer, on
cherchera ? privilegier la respiration ana?robie h?t?rotrophe qui exige
une source organique de carbone combustible qui
peut ?tre du M?thanol, du Glucose ou tout simplement les d?chets organiques
du milieu
: cadavres, exc?s de nourriture etc... pour
?viter les complications li?es ? l?existence de fermentations dans les
zones ana?robies avec productions possibles de M?thane, d?Hydrog?ne sulfur?.
Par ailleurs ces ?tres vivants n?cessitent ?galement entre autres choses
une source de phosphore.
Il sera possibled'en rajouter sous la forme d?hydrog?nophosphate
de sodium ou de potassium
(Lavigne 1993)
mais la plupart du temps la pr?sence de phosphates dans l'aquarium est suffisante
pour faciliter cette denitrification
h?t?rotrophe.
Ceci
explique la diminution des phosphates lors de l'utilisation de concentr?s
bact?riens bien ?labor?s..
Voil?
le principe d'action de l'?puration biologique.
Pour
en savoir plus : www.prodibio.fr